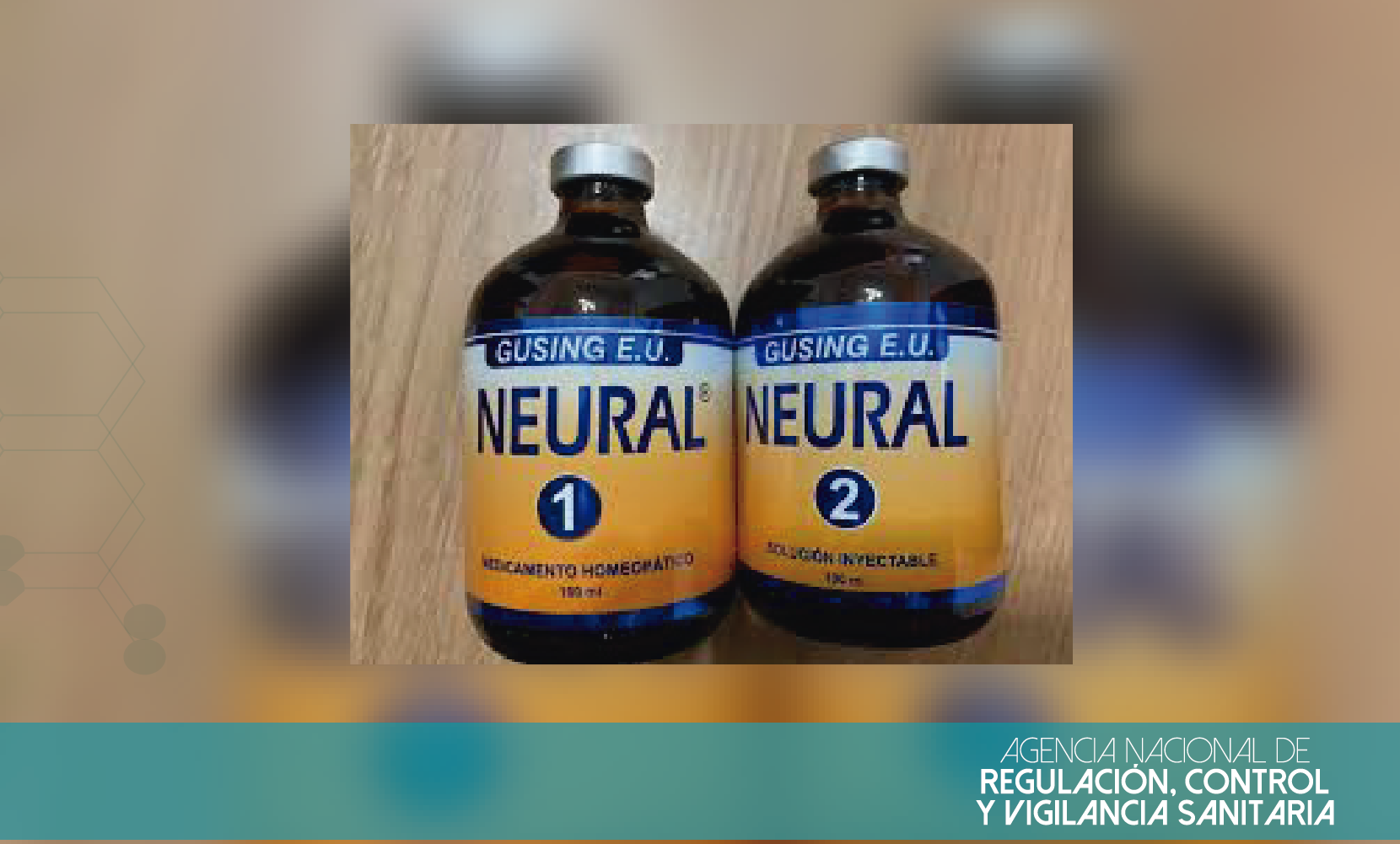
Alerta sobre circulación de producto NEURAL SOLUCIÓN INYECTABLE falsificado
Fecha de publicación: 02/12/2020
La Agencia Nacional de Regulación, Control y Vigilancia Sanitaria (Arcsa) da a conocer a la población ecuatoriana la alerta sobre el producto NEURAL SOLUCIÓN INYECTABLE (Procaína 2%) de la empresa GUSIN E.U.
La empresa GFPHARMA ECUADOR S.A. notificó a ARCSA que «dentro de nuestras actividades diarias de visita y promoción de nuestros productos en consultorios y punto de venta, detectamos la presencia de un medicamento con un nombre similar a uno de nuestra propiedad y marca registrada; producto que en sus dos presentaciones registradas no corresponde desde
ningún punto de vista al dossier entregado a la autoridad para la obtención del Registro Sanitario vigente».
Los datos de análisis son los siguientes:
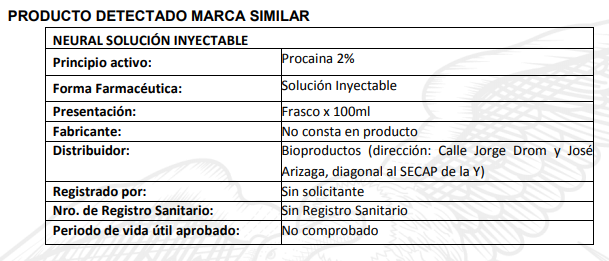
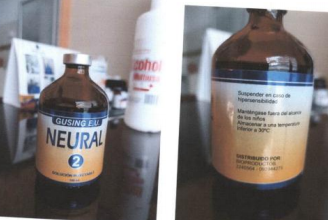
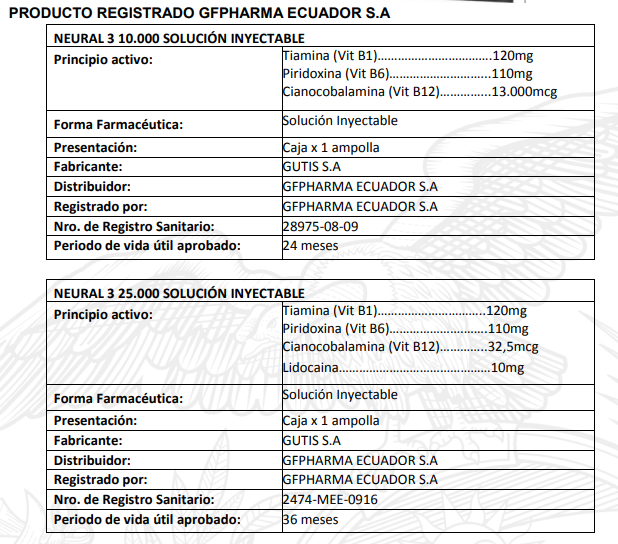
Como podemos observar de la información procedente, los dos productos no son iguales bajo ningún criterio de análisis, así como tampoco el efecto terapéutico en pacientes es el mismo, pues sus principios activos difieren totalmente.
Situación en Ecuador:
El producto NEURAL SOLUCIÓN INYECTABLE indicado en la alerta no se evidencia en la base de datos de Medicamentos.
En este sentido, Arcsa hace un llamado a la población para que se abstenga de adquirir y consumir el producto NEURAL SOLUCIÓN INYECTABLE, con las características indicadas en la alerta comunicada por la empresa GFPharma Ecuador S.A, y de evidenciarse su comercialización deberá notificarlo inmediatamente.
La Agencia invita a la ciudadanía a adquirir medicamentos que tengan Registro Sanitario ecuatoriano vigente, y que estos sean únicamente adquiridos en establecimientos autorizados; a su vez informar sobre la venta o distribución del lote del producto objeto de la alerta a través del
correo control.posterior@controlsanitario.gob.ec o por medio de la aplicación Arcsa Móvil; así como cualquier evento adverso relacionado con medicamentos al correo electrónico farmaco.vigilancia@controlsanitario.gob.ec
Sus datos personales y la información proporcionada serán estrictamente confidenciales.
