Retiro voluntario de lotes de producto RANITIDINA GENFAR SOLUCIÓN INYECTABLE
Fecha de publicación: 13/03/2020
La Agencia Nacional de Regulación, Control y Vigilancia Sanitaria (Arcsa) ha tomado conocimiento mediante la empresa SANOFI-AVENTIS DEL ECUADOR S.A. del retiro voluntario del producto RANITIDINA GENFAR SOLUCIÓN INYECTABLE 50mg/2ml con Registro Sanitario GBE-1032-04-07.
SANOFI-AVENTIS DEL ECUADOR S.A. ha comunicado a la Agencia que tomó la propuesta de retiro voluntario del mercado como medida de precaución debido a la posible contaminación con una impureza de nitrosamina llamada N-Nitrosodimetilamina (NDMA). La empresa ha identificado que los lotes vigentes comercializados pueden potencialmente contener esta inesperada impureza.
SANOFI-AVENTIS DEL ECUADOR S.A. confirma que no hay otros lotes de producto que se vean afectados por este retiro del mercado.
A continuación, se detalla la lista de los lotes del producto RANITIDINA GENFAR SOLUCIÓN INYECTABLE 50mg/2ml afectados por el retiro voluntario:
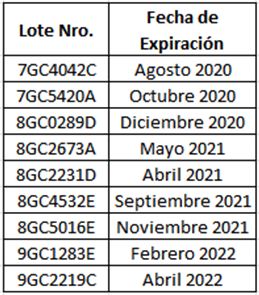
Ante lo expuesto, Arcsa recomienda:
A LOS ESTABLECIMIENTOS DE SALUD:
1. Absténgase de utilizar los lotes del medicamento objeto del retiro voluntario.
2. Ponga en cuarentena los lotes del medicamento referenciado y comuníquese con el importador, distribuidor o comercializador.
3. Reporte los eventos adversos asociados a la utilización del medicamento involucrado al Centro Nacional de Farmacovigilancia de Arcsa, al correo farmaco.vigilancia@controlsanitario.gob.ec
A LOS ESTABLECIMIENTOS DISTRIBUIDORES Y COMERCIALIZADORES:
1. No utilizar, distribuir ni comercializar los lotes afectados del medicamento RANITIDINA GENFAR SOLUCIÓN INYECTABLE 50mg/2ml objeto del Retiro Voluntario.
2. De identificar los lotes antes mencionados, ponerlo en cuarentena e informe inmediatamente a Arcsa.
3. Facilitar el proceso de retiro del mercado ejecutado por la empresa SANOFI-AVENTIS del Ecuador S.A.
A LA COMUNIDAD EN GENERAL:
1. No utilizar los lotes afectados del producto objeto del retiro voluntario, como medida de precaución debido a los posibles riesgos que pueden representar para su salud.
2. A la población que está bajo tratamiento con medicamentos que contienen Ranitidina de los lotes mencionados en la presente alerta, acudir a su médico tratante para considerar otras alternativas con las mismas indicaciones terapéuticas.
Arcsa invita a la ciudadanía a informar sobre la venta o distribución de los lotes del medicamento objeto del retiro voluntario a través del correo control.posterior@controlsanitario.gob.ec o por medio de la aplicación Arcsa Móvil; así como cualquier evento o incidente adverso relacionado con los medicamentos al correo electrónico farmaco.vigilancia@controlsanitario.gob.ec
Sus datos personales y la información proporcionada serán estrictamente confidenciales.